- Avtor Alex Aldridge aldridge@what-difference.com.
- Public 2023-12-17 13:49.
- Nazadnje spremenjeno 2025-06-01 07:37.
Ključna razlika med dušikovim monoksidom in dušikovim pentoksidom je, da je dušikov monoksid brezbarven plin, medtem ko je dušikov pentoksid bela trdna snov.
Dušikov monoksid in dušikov pentoksid sta kemični spojini, ki vsebujeta dušik in kisik. To so dušikovi oksidi. Vendar pa imajo različne kemijske in fizikalne lastnosti.
Kaj je dušikov monoksid?
Dušikov monoksid je anorganska spojina s kemijsko formulo NO. Imenujemo ga dušikov oksid, ker je dušikov oksid. Pravzaprav je prosti radikal, ker ima nesparjen elektron. Poleg tega je heteronuklearna dvoatomna molekula.
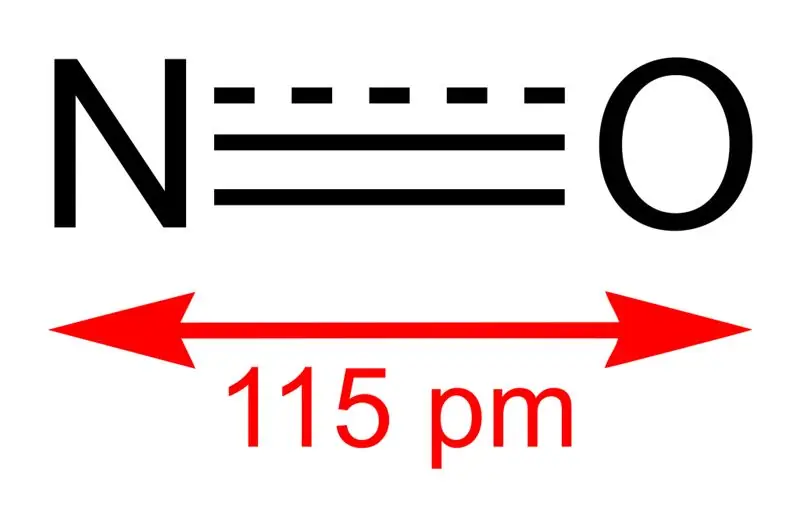
Slika 01: Struktura dušikovega monoksida in dolžina vezi med N in O
Molska masa te spojine je 30 g/mol. Pojavlja se kot brezbarven plin. Poleg tega je njegovo tališče −164 °C, medtem ko je vrelišče −152 °C, kar sta zelo majhni vrednosti v primerjavi z vrednostmi drugih dušikovih oksidov. Ta prosti radikal lahko proizvedemo z oksidacijo amoniaka pri 850 °C v prisotnosti platinskega katalizatorja. Vendar pa ga v laboratorijskem merilu lahko pripravimo z redukcijo razredčene dušikove kisline z bakrom.
Kaj je dušikov pentoksid?
Dušikov pentoksid je anorganska spojina s kemijsko formulo N2O5 Imenujemo ga dušikov pentoksid. Je binarni dušikov oksid. Poleg tega je nestabilen in lahko deluje kot nevaren oksidant. Molska masa spojine je 108,01 g/mol. Pojavlja se kot bela trdna snov.
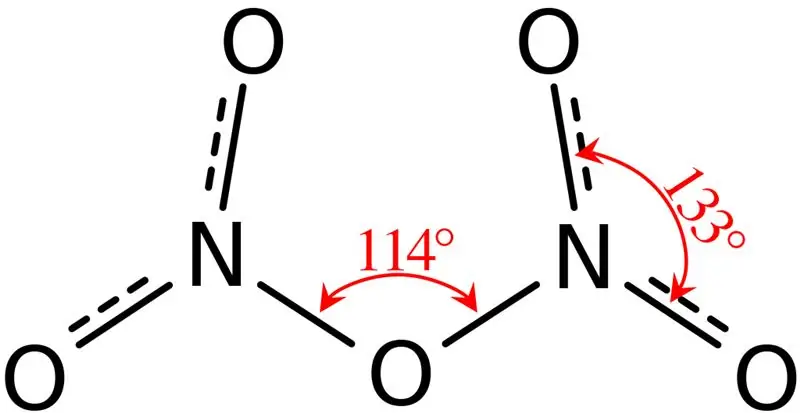
Slika 02: Struktura dušikovega pentoksida
Poleg tega je tališče te spojine 41 °C in pri 47 °C je ta spojina sublimirana. Ta spojina reagira z vodo in daje dušikovo kislino. Poleg tega je molekularna oblika molekule dušikovega pentoksida ravna. To spojino lahko proizvedemo z dehidracijo dušikove kisline s fosforjevim pentoksidom.
Kakšna je razlika med dušikovim monoksidom in dušikovim pentoksidom?
Dušikov monoksid je anorganska spojina s kemijsko formulo NO, medtem ko je dušikov pentoksid anorganska spojina s kemijsko formulo N2O5 Ključna razlika med dušikovim monoksidom in dušikovim pentoksidom je, da je dušikov monoksid brezbarven plin, medtem ko je dušikov pentoksid bela trdna snov. Poleg tega lahko proizvedemo dušikov monoksid z oksidacijo amoniaka pri 850 °C v prisotnosti platinskega katalizatorja. Vendar pa proizvodnja dušikovega pentoksida poteka z dehidracijo dušikove kisline s fosforjevim pentoksidom. Če upoštevamo molekularno obliko, je dušikov monoksid linearen, medtem ko je dušikov pentoksid ravninski.
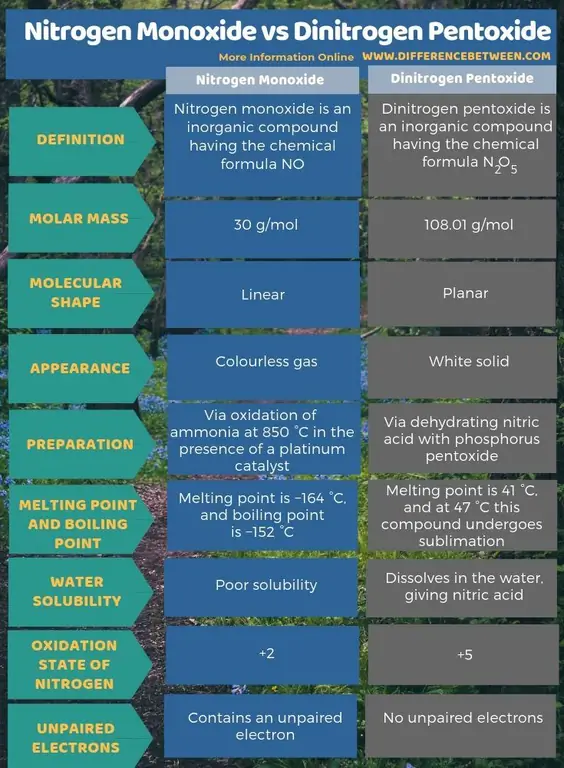
Povzetek - Dušikov monoksid proti dušikovemu pentoksidu
Dušikov monoksid je anorganska spojina s kemijsko formulo NO, medtem ko je dušikov pentoksid anorganska spojina s kemijsko formulo N2O5 Ključna razlika med dušikovim monoksidom in dušikovim pentoksidom je, da je dušikov monoksid brezbarven plin, medtem ko je dušikov pentoksid bela trdna snov.






